Введение
В эстетической хирургии понятие нормы весьма условно и, в то же время, вполне конкретно непосред ственно для пациента. Однако мало кто будет спорить с тем фактом, что состояния, сопровождающиеся вы раженным дефицитом объёма молочных желез, далеки от нормы. Объединяя эти нарушения общим тер мином – гипомастия, мы имеем в виду лишь внешнюю эстетическую составляющую, опуская индивидуаль ные морфофункциональные особенности и причин ные факторы. Основываясь на метрических парамет рах молочных желез, существующие классификации носят больше прикладной характер, нежели клини ческий. С хирургической точки зрения такой подход вполне объясним и оправдан, однако этого не всегда достаточно для построения полноценного диагноза.
Отдельные состояния, сопровождающиеся гипо мастией в рамках врожденных и эндокринных синд ромов и заболеваний, изучены и описаны в литерату ре достаточно подробно [1, 5, 6, 10, 14], однако, об щей этиопатогенетической систематизации состоя ний, характеризующихся дефицитом объёма тканей молочных желез на данный момент нет. По нашему мнению, этому есть несколько причин:
- отсутствие четких этиопатогенетических крите риев гипомастии;
- сложность и малоизученность тонких механизмов регуляции развития молочных желез;
- многообразие факторов, приводящих к наруше нию этих механизмов;
- высокая вариабельность морфологических ха рактеристик не только у разных женщин, но у од ной и той же в разные периоды жизни и цикла.
В своём исследовании мы попытались оценить группу пациентов с выраженной гипомастией с пози ций этиопатогенеза и, исходя из результатов, сфор мулировать наиболее общие аспекты систематиза ции данных нарушений и построения диагноза.
Материалы и методы
В исследование мы включили две группы пациен тов. В первую, основную группу, мы включили 38 па циенток с выраженной гипомастией, которым была выполнена первичная увеличивающая маммопласти ка. Во вторую группу, которую мы рассматривали как контрольную, мы включили 31 пациентку, которым также была выполнена первичная увеличивающая маммопластика. Критериями отбора пациенток в ос новную группу стали: выраженный одно или двухсто ронний дефицит объёма тканей молочных желез, со храненный сосковоареолярный комплекс и отсутст вие четко визуализируемой субмаммарной дуги или складки. В контрольную группу мы включили пациен ток с умеренной гипомастией без птоза.
Анализ пациентов проводили ретроспективно. Оце нивали наличие и характер врожденных дефектов и пороков развития, гормональных нарушений, функ циональное состояние молочных желез, общее физи ческое развитие, сопутствующие и перенесенные за болевания. Оценку проводили на основании анам нестических данных и данных физикального обследо вания пациенток. При необходимости и по показани ям дополнительно производили инструментальные и лабораторные исследования. В анализе результатов исследования решающее значение придавалось установленной и описанной в литературе связи неко торых выявленных дефектов развития и сопутствую щих заболеваний с гипомастией [5, 8–11].
В основу систематизации так же положены три ос новных понятия: гипомастия, гипоплазия и гипотрофия.
Результаты и обсуждение
Возраст пациенток, оперированных по поводу гипо мастии и вошедших в исследование, колебался от 18 до 42 лет. Средний возраст пациенток основной груп пы составил 27 лет, контрольной – 30 лет.
В основной группе семь пациенток имели выра женную одностороннюю гипомастию с асимметрией молочных желез. Причина гипомастии у четверых из них – хирургическое вмешательство на грудной клет ке в области одной из молочных желез – три наблю дения (рис. 1), и лучевая терапия в детском возрас те – одно наблюдение (рис. 2). Односторонняя гипо
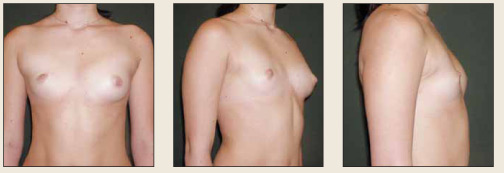
Рис. 1. Пациентка Н., 22 года, вторичная ятрогенная гипомастия справа, вторичная приобретенная асимметрия молочных желез, в возрасте 8 мес оперирована по поводу гемангиомы правой молочной железы Fig. 1. Patient N., aged 22 years, with righthand side secondary iatrogenic hypomastia and secondary acquired breast asymmetry. The patient was operated at the age of 8 years for right breast hemangioma
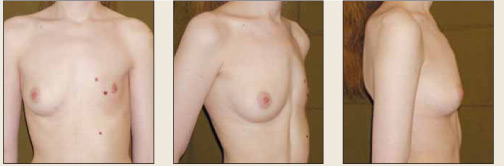
Рис. 2. Пациентка П., 20 лет, вторичная ятрогенная гипоплазия молочной железы справа, вторичная приобретенная асимметрия молочных желез, лучевая терапия в детском возрасте Fig. 2. Patient P., aged 20 years, secondary iatrogenic hypoplasia of the right breast and secondary acquired breast asymmetry. The patient underwent radiotherapy when a child
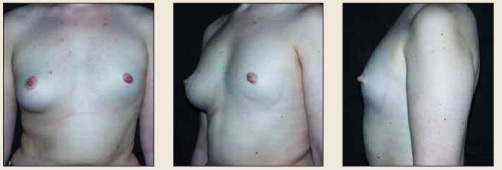
Рис. 3. Пациентка Б., врожденная гипомастия справа, врожденная асимметрия молочных желез Fig. 3. Patient B. with righthand side congenital hypomastia and congenital breast asymmetry
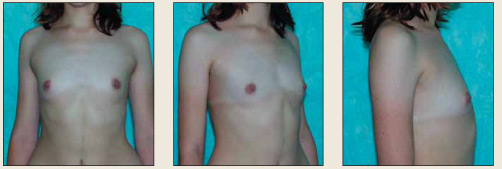
Рис. 4. Пациентка А., 18 лет, первичная гипомастия, диффузное увеличение щитовидной железы II степени, эутиреоз, гиперандрогения, генитальный инфантилизм Fig. 4. Patient A., aged 18 years, with primary hypomastia, grade II diffuse enlargement of the thyroid gland, euthyroidism,
hyperandrogenism, and genital infantilism
мастия у остальных трех пациенток была врожденно го генеза (рис. 3).
Оценивая функциональное состояние молочных желез пациенток обеих групп, надо отметить, что из 17 (45 %) рожавших пациенток основной группы не смотря на выраженный дефицит объёма тканей мо лочных желез – только у двух не было лактации. В кон трольной группе никто из 23 (74%) пациенток, имею щих детей, на отсутствие лактации не жаловался.
Обращает на себя внимание тот факт, что количест во родов доношенным плодом в группе выраженных гипомастий – заметно ниже. Это могло бы свидетель ствовать о возможных гормональных нарушениях и незрелости репродуктивной системы, однако, мы не склонны придавать этому решающее значение, учи тывая, что данные могут несколько искажаться факто рами социального и психологического плана, играю щими особую роль в жизни пациенток с выраженным дефицитом объёма молочных желез [4].
В одном наблюдении у пациентки 18 лет, включен ной в основную группу, выявлена эндокринная пато логия с нарушением гормонального статуса в виде гиперандрогении и изменения уровня оборотных гор монов щитовидной железы, приведшая к дисгормо нальному половому развитию, половому инфантилиз му и микромастии (рис. 4). В данном наблюдении вы явлен эутиреоз с диффузным увеличением щитовид ной железы II степени, по поводу чего пациентка на блюдалась у эндокринолога. Надо отметить, что именно в период полового созревания любые нару шения нейрогуморального гомеостаза крайне пагуб но влияют на половое развитие и развитие молочных желез в частности [1, 2]. Хорошей иллюстрацией тому служит пример двух пациенток контрольной группы
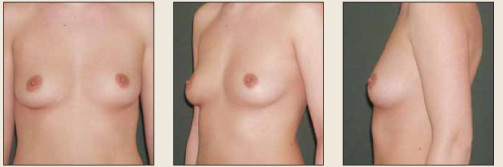
Рис. 5. Пациентка В., 28 лет, эстетическая гипомастия, сопутствующая патология – узловой эутиреоидный зоб, выявлен к 28 годам Fig. 5. Patient C., aged 28 years, with aesthetically unacceptable hypomastia and concurrent euthyroid nodular goiter diagnosed at the age of 28 years
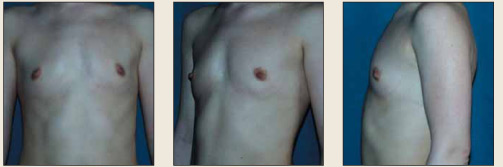
Рис. 6. Пациентка Б., 26 лет, эстетическая гипомастия, туберкулёз лимфоузлов в анамнезе Fig. 6. Patient B., aged 26 years, with aesthetically unacceptable hypomastia and the history of lymph node tuberculosis
28 и 32 лет с патологией щитовидной железы, забо левших уже будучи взрослыми и не имеющих значи тельного нарушение объёма молочных желез (рис. 5).
О возможности влияния тяжелых инфекционных (особенно вирусных) и системных заболеваний, нару шений обменных процессов, интоксикаций, травм ЦНС в период активного становления репродуктив ной системы на половое развитие сообщали многие авторы [1, 2, 3]. Анализ анамнестических данных на ших пациенток в разумной степени подтверждает это утверждение. В основной группе шесть пациенток в возрасте 10–16 лет перенесли туберкулёз лимфати ческих узлов (рис. 6), гепатит «В», гепатит «А», пнев монию, корь, ревмокардит. Невозможно с полной уве ренностью утверждать, что именно эти болезни яви лись причиной гипомастии, однако, подобных приме ров в контрольной группе мы не нашли.
Подобным образом патогенные и наследственные факторы могут воздействовать и на фетальные ткани плода, вызывая множественные врожденные и наслед ственные дефекты, в том числе и молочных желез. В ос нове этих синдромов лежат различного рода диспла зии, чаще эктодермальная и мезенхимальная. Их тяже лые формы крайне редки, а субклинические случаи имеют стёртую симптоматику и сложны в диагностике. В литературе описываются случаи врожденных гипо мастий в сочетании с другими врожденными дефекта ми костной и соединительной ткани, кожи и её произ водных [10, 11, 13, 14]. В наше исследование мы вклю чили пациенток без грубой врожденной патологии, учи тывая при этом любые признаки врожденности, сочета ющиеся с гипомастией и описанные в литературе. Ре шающее значение имели костные деформации грудно го скелета (особенно экскавация грудины, в меньшей степени её килевидная деформация, еще меньше ки фоз, сколиоз, «синдром прямой спины»), пролапс мит рального клапана, дефекты кожи (многочисленные пиг ментные пятна типа веснушек), наличие семейного анамнеза гипомастии. Так же к нарушениям врожденно го генеза мы относим односторонние гипомастии при условии отсутствия воздействия на маммогенез внеш них повреждающих факторов. Самая распространенная деформация в обеих группах – сколиоз (42 и 32 %). Хо тя в основной группе этот процент выше, мы не стали придавать этому большого значения. Гораздо более важным оказалось наличие у пяти пациенток основной группы деформаций грудины по типу экскавации и у од ной – килевидной, а так же наличие подтвержденного пролапса митрального клапана у трёх пациенток и мно жественной кожной пигментации по типу веснушек у двух пациенток (рис. 7–9). У одной пациентки основной группы гипомастия носила явный семейный характер. В контрольной группе нами выявлена только килевидная деформация грудины у трех пациенток.
Анализируя данные результаты, можно сделать одно значный вывод, частота врожденных дефектов в направ лении «умеренная гипомастия – выраженная гипомас тия – микромастия» увеличивается. Соответственно до ля гипомастий, имеющих врожденный генез, увеличи вается в том же направлении. Это утверждение верно в том случае, если дефицит тканей молочных желез свя зан с сопутствующим врожденным дефектом патогене тически. Интересен тот факт, что в основной группе вы явлен более неблагоприятный семейный анамнез по раку молочной железы (четыре пациентки против одной в контрольной группе). Это так же может свидетельство
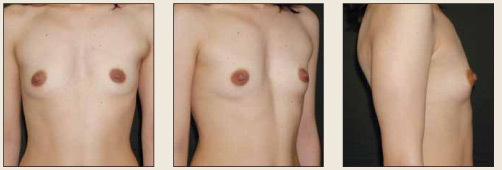
Рис. 7. Пациентка Л., 32 года, врожденная гипомастия, экскавация нижней трети грудины, нормальная функция молочных желез Fig. 7. Patient L., aged 32 years, with congenital hypomastia, excavation of the lower third of the sternum and normal function of mammary glands
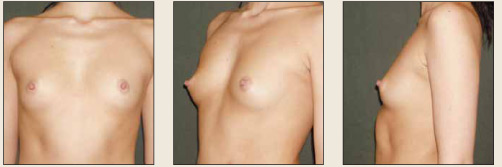
Рис. 8. Пациентка З., 22 года, врожденная гипомастия, пролапс митрального клапана, правосторонний неротационный сколиоз Fig. 8. Patient Z., aged 22 years, with congenital hypomastia, mitral valve prolapse, and righthand side nonrotational scoliosis
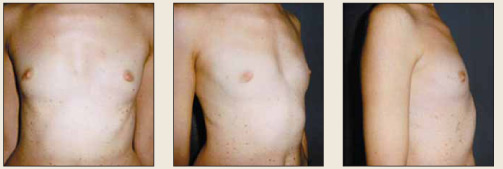
Рис. 9. Пациентка С., 31 год, врожденная гипомастия, пролапс митрального клапана, множественные пигментные пятна, в семейном анамнезе рак молочной железы Fig. 9. Patient S., aged 31 years, with congenital hypomastia, mitral valve prolapse, multiple pigmentary spots, and breast cancer in the family history
вать о большей роли врожденных и генетических факто ров в патогенезе выраженных гипомастий.
У всех пациенток с врожденной гипомастией в обе их группах имеющих детей сохранена способность к лактации. Повидимому, это связано с тем, что собст венно железистая ткань сохраняет свою функцию, а дефицит объёма больше связан с дефицитом соеди нительнотканного компонента железы.
У основной массы пациентов обеих групп отсутство вали какиелибо иные отклонения, кроме гипомастии. Большая часть из них обратилась с жалобами на уменьшение объёма и ухудшение формы желез после родов и лактации. Это связано с инволютивной гипот рофией молочных желез, в основе которой лежит пре обладание процессов апоптоза, обратной дифферен цировки железистой ткани, редукции перигландулярной стромы и замещения железистой ткани жировой. Уже начиная с 25 летнего возраста, у рожавших жен щин в молочных железах преобладают процессы ин волюции, а к 40 годам они отмечаются как у рожавших, так и у нерожавших женщин. В этой связи инволютив ную гипотрофию принято делить на постлактационную и возрастную. Однако существует группа пациенток с дефицитом объёма молочных желез, которые, не имея явных признаков врожденной патологии, нару шений гормонального статуса, задержки полового развития или инволютивных изменений, по сути, оста ются за рамками нашей систематизации. Нарушени ям такого типа мы дали определение идиопатической гипоплазии (при условии нарушенной функции желе зы) или эстетической гипомастии (в случае если фун кция сохранена) (рис. 10) и выделили в отдельную категорию – дефицит объёма молочных желез неуста новленного генеза.
В итоге, пациенток каждой группы мы разделили на 5 категорий гипомастии (1я категория – ассоцииро ванная с другими врожденными дефектами развития или имеющая наследственный характер
(одно или двухсторонняя); 2я – ассоциированная с наруше нием или задержкой полового развития, или наруше нием нейрогуморального гомеостаза; 4я – без явных признаков врождённой патологии, нарушения гормо нального статуса или полового развития, инволютив ных изменений (см. таблицу).
Под понятием гипомастия мы понимаем только де фицит объёма тканей молочной железы. Говоря о ги поплазии, мы имеем в виду комплекс признаков: де фицит объёма, морфологическую незрелость тканей и нарушение функции. В ситуациях, когда невозмож но оценить морфофункциональное состояние молоч ной железы, мы допускаем применение термина ги помастия.
Таким образом, основу контрольной группы соста вили пациентки с постлактационной инволютивной гипотрофией. Большую же часть основной группы заняли пациентки с врожденной гипомастией и в мень шей степени с постлактационной инволютивной ги потрофией.
Таблица. Распределение пациентов основной и контрольной групп по категориям
Выводы
Проводя ретроспективный анализ небольшой группы пациентов, оперированных по поводу дефи цита объёма молочных желез, мы не могли получить более точные результаты, чем те, которые пред ставлены в нашем исследовании. Однако и эти ре зультаты позволяют сделать некоторые выводы, первый и главный из которых состоит в том, что вы раженной гипомастии чаще сопутствует врожден ная патология. Несмотря на единственный выяв ленный случай первичной гипомастии, при более тщательном исследовании гормонального статуса наших пациентов, возможно, их оказалось бы боль ше. Даже на основании анамнестических и физи кальных данных можно определить пациентку в ту или иную группу гипомастии, обосновать и сформу лировать полноценный диагноз. При выраженном дефиците объёма тканей молочных желез и, осо бенно при микромастии, чаще всего имеется при чина этого дефекта. К сожалению, не всегда воз можно достоверно её установить, но можно конста тировать её существование. Этот вопрос требует более фундаментального изучения и, несомненно, большой вклад в понимание механизмов формиро вания, развития молочных желез и, собственно па тогенеза, внесут последние исследования в облас ти человеческого генома, молекулярной биологии и факторов роста. На данный же момент реальной альтернативы хирургическому лечению гипомастии мы не видим. Однако всегда надо учитывать, что ги помастия, а особенно микромастия, могут быть проявлением соматического патологического про цесса, что в корне может повлиять на принятие ре шения об эстетической коррекции данных состоя ний молочных желез.
ЛИТЕРАТУРА
Коколина В.Ф.
Гинекологическая эндокринология детско го и подросткового возраста: Руководство для врачей / 4е изд., перераб., доп. – М.: ИД МЕДПРАКТИКАМ, 2005, 340 с.
Малыхина Т.В.
Отдельные физиологические аспекты вли яния гормонов на процессы в молочных железах // Вестник СамГУ – Естественнонаучная серия. – 2006. – № 6/2 (46). – 178–188 с.
Сметник В.П.
Половые гормоны и молочная железа (обзор литературы) // Гинекология. – Т. 2. – № 5. – 2000.
Маммопластика при нарушениях объёма и формы молоч ной железы / В.М. Тимербулатов, О.С. Попов, В.В. Плечев, О.В. Попова. – М.: ТриадаХ, 2002. – 176 с.
Coumoul X., ChuXia Deng.
Roles of FGF Receptors in
Mammalian Development and Congenital Diseases // Birth Defects Res. – (Part C). – V. 69. – P. 286–304. – 2003
Foley J, Dann P, Hong J, Cosgrove J, Dreyer B, Rimm D, et al.
Parathyroid hormonerelated protein maintains mammary еpithe lial fate and triggers nipple skin differentiation during embryonic breast development // Development 2001;128: 513–25.
Herynk Matthew H., Ph.D, and Fuqua Suzanne A. W., Ph. D.
Estrogen Receptor Mutations in Human Disease // Endocr. Rev.
–
Vol. 25: 869898. – Dec. – 2004.
8.
Ishida L.H., Alves H.R.N., Munhoz A.M., Kaimoto C., Ishida L.C., Saito F.L., Gemperlli R., Ferreira M.C.
Athelia: case report and review of the literature// British Journal of Plastic Surgery (2005) 58, 833–837
Lin, K.Y., Nguyen, D.B., and Williams, R.M.
Complete breast absence revisited // Plast. Reconstr. Surg. 106: 98, 2000
Malcolm A. D.
Mitral valve prolapse associated with other dis orders. Casual coincidence, common link, or fundamental genetic disturbance? // Br. Heart J. 1985 April; 53(4): 353–362
Rosenberg C.A., Derman G.H., Grabb W.C., Buda A.J.
Hypomastia and mitralvalve prolapse. Evidence of a linked embryologic and mesenchymal dysplasia. // N. Engl. J. Med. 1983; 309:12302.
Sadove A.M., Van Aalst J.A.
Congenital and Acquired Pediatric Breast Anomalies// Plastic and reconstructive surgery,
2005, April 1, p. 10391050.
Strewler Gordon J., M.D.
The Physiology of Parathyroid HormoneRelated Protein // The NEW ENGLAND JOURNAL of MEDICINE Vol. 342:177185
Wysolmerski John J., Cormier Sarah, Philbrick William M., Dann Pamela, Zhang JianPing, Roume Joelle, Delezoide Anne Lise and Silve Caroline
Absence of Functional Type 1 Parathyroid Hormone (PTH)/PTHRelated Protein Receptors in Humans Is Associated with Abnormal Breast Development and Tooth Impaction // The Journal of Clinical Endocrinology Metabolism.
–
Vol. 86. – № 4. – Р. 17881794. – 2001.
Гипомастия: принципы систематизации и построения диагноза
Акад. РАМН проф. Н.О. МИЛАНОВ1, О.Л. НИКИТИН, А.Г. ЛИ, Ю.В. БЕЛОВА, Л.Г. КОРНИЕНКО ГУ РНЦХ им. акад. Б.В. Петровского РАМН
Введение
В эстетической хирургии понятие нормы весьма условно и, в то же время, вполне конкретно непосред ственно для пациента. Однако мало кто будет спорить с тем фактом, что состояния, сопровождающиеся вы раженным дефицитом объёма молочных желез, дале ки от нормы. Объединяя эти нарушения общим тер мином – гипомастия, мы имеем в виду лишь внешнюю эстетическую составляющую, опуская индивидуаль ные морфофункциональные особенности и причин ные факторы. Основываясь на метрических парамет рах молочных желез, существующие классификации носят больше прикладной характер, нежели клини ческий. С хирургической точки зрения такой подход вполне объясним и оправдан, однако этого не всегда достаточно для построения полноценного диагноза.
Отдельные состояния, сопровождающиеся гипо мастией в рамках врожденных и эндокринных синд ромов и заболеваний, изучены и описаны в литерату ре достаточно подробно [1, 5, 6, 10, 14], однако, об щей этиопатогенетической систематизации состоя ний, характеризующихся дефицитом объёма тканей молочных желез на данный момент нет. По нашему мнению, этому есть несколько причин:
• отсутствие четких этиопатогенетических крите риев гипомастии;
1Н.О. МИЛАНОВ Россия, 119992, Москва, Абрикосовский пер., 2 Тел: (495) 248 16 15, факс: (495) 248 60 77 Email: milanov@med.ru
Hypomastia: principles of systematization and diagnosis
Professor N.O. MILANOV1, member of Russian Academy of Medical Sciences, O.L NIKITIN, A.G. LEE, Yu.V. BELOVA,
L.G. KORNIENKO
B.V. Petrovsky State Research Centre of Surgery, Russian Academy of Medical Sciences
- сложность и малоизученность тонких механизмов регуляции развития молочных желез;
- многообразие факторов, приводящих к наруше нию этих механизмов;
- высокая вариабельность морфологических ха рактеристик не только у разных женщин, но у од ной и той же в разные периоды жизни и цикла.
В своём исследовании мы попытались оценить группу пациентов с выраженной гипомастией с пози ций этиопатогенеза и, исходя из результатов, сфор мулировать наиболее общие аспекты систематиза ции данных нарушений и построения диагноза.
Материалы и методы
В исследование мы включили две группы пациен тов. В первую, основную группу, мы включили 38 па циенток с выраженной гипомастией, которым была выполнена первичная увеличивающая маммопласти ка. Во вторую группу, которую мы рассматривали как контрольную, мы включили 31 пациентку, которым также была выполнена первичная увеличивающая маммопластика. Критериями отбора пациенток в ос новную группу стали: выраженный одно или двухсто ронний дефицит объёма тканей молочных желез, со храненный сосковоареолярный комплекс и отсутст вие четко визуализируемой субмаммарной дуги или
1N.O. Milanov Abrikosovsky per., 2, 119992 Moscow, Russia Tel.: (495) 248 16 15; fax: (495) 248 60 77 email: milanov@med.ru
складки. В контрольную группу мы включили пациен ток с умеренной гипомастией без птоза.
Анализ пациентов проводили ретроспективно. Оце нивали наличие и характер врожденных дефектов и пороков развития, гормональных нарушений, функ циональное состояние молочных желез, общее физи ческое развитие, сопутствующие и перенесенные за болевания. Оценку проводили на основании анам нестических данных и данных физикального обследо вания пациенток. При необходимости и по показани ям дополнительно производили инструментальные и лабораторные исследования. В анализе результатов исследования решающее значение придавалось установленной и описанной в литературе связи неко торых выявленных дефектов развития и сопутствую щих заболеваний с гипомастией [5, 8–11].
В основу систематизации так же положены три ос новных понятия: гипомастия, гипоплазия и гипотрофия.
Результаты и обсуждение
Возраст пациенток, оперированных по поводу гипо мастии и вошедших в исследование, колебался от 18 до 42 лет. Средний возраст пациенток основной груп пы составил 27 лет, контрольной – 30 лет.
В основной группе семь пациенток имели выра женную одностороннюю гипомастию с асимметрией молочных желез. Причина гипомастии у четверых из них – хирургическое вмешательство на грудной клет ке в области одной из молочных желез – три наблю дения (рис. 1), и лучевая терапия в детском возрас те – одно наблюдение (рис. 2). Односторонняя гипо

Рис. 1. Пациентка Н., 22 года, вторичная ятрогенная гипомастия справа, вторичная приобретенная асимметрия молочных желез, в возрасте 8 мес оперирована по поводу гемангиомы правой молочной железы Fig. 1. Patient N., aged 22 years, with righthand side secondary iatrogenic hypomastia and secondary acquired breast asymmetry. The patient was operated at the age of 8 years for right breast hemangioma

Рис. 2. Пациентка П., 20 лет, вторичная ятрогенная гипоплазия молочной железы справа, вторичная приобретенная асимметрия молочных желез, лучевая терапия в детском возрасте Fig. 2. Patient P., aged 20 years, secondary iatrogenic hypoplasia of the right breast and secondary acquired breast asymmetry. The patient underwent radiotherapy when a child Рис. 3. Пациентка Б., врожденная гипомастия справа, врожденная асимметрия молочных желез Fig. 3. Patient B. with righthand side congenital hypomastia and congenital breast asymmetry


Рис. 4. Пациентка А., 18 лет, первичная гипомастия, диффузное увеличение щитовидной железы II степени, эутиреоз, гиперандрогения, генитальный инфантилизм Fig. 4. Patient A., aged 18 years, with primary hypomastia, grade II diffuse enlargement of the thyroid gland, euthyroidism,
hyperandrogenism, and genital infantilism
мастия у остальных трех пациенток была врожденно го генеза (рис. 3).
Оценивая функциональное состояние молочных желез пациенток обеих групп, надо отметить, что из 17 (45 %) рожавших пациенток основной группы не смотря на выраженный дефицит объёма тканей мо лочных желез – только у двух не было лактации. В кон трольной группе никто из 23 (74%) пациенток, имею щих детей, на отсутствие лактации не жаловался.
Обращает на себя внимание тот факт, что количест во родов доношенным плодом в группе выраженных гипомастий – заметно ниже. Это могло бы свидетель ствовать о возможных гормональных нарушениях и незрелости репродуктивной системы, однако, мы не склонны придавать этому решающее значение, учи тывая, что данные могут несколько искажаться факто рами социального и психологического плана, играю щими особую роль в жизни пациенток с выраженным дефицитом объёма молочных желез [4].
В одном наблюдении у пациентки 18 лет, включен ной в основную группу, выявлена эндокринная пато логия с нарушением гормонального статуса в виде гиперандрогении и изменения уровня оборотных гор монов щитовидной железы, приведшая к дисгормо нальному половому развитию, половому инфантилиз му и микромастии (рис. 4). В данном наблюдении вы явлен эутиреоз с диффузным увеличением щитовид ной железы II степени, по поводу чего пациентка на блюдалась у эндокринолога. Надо отметить, что именно в период полового созревания любые нару шения нейрогуморального гомеостаза крайне пагуб но влияют на половое развитие и развитие молочных желез в частности [1, 2]. Хорошей иллюстрацией тому служит пример двух пациенток контрольной группы

Рис. 5. Пациентка В., 28 лет, эстетическая гипомастия, сопутствующая патология – узловой эутиреоидный зоб, выявлен к 28 годам Fig. 5. Patient C., aged 28 years, with aesthetically unacceptable hypomastia and concurrent euthyroid nodular goiter diagnosed at the age of 28 years

Рис. 6. Пациентка Б., 26 лет, эстетическая гипомастия, туберкулёз лимфоузлов в анамнезе Fig. 6. Patient B., aged 26 years, with aesthetically unacceptable hypomastia and the history of lymph node tuberculosis
28 и 32 лет с патологией щитовидной железы, забо левших уже будучи взрослыми и не имеющих значи тельного нарушение объёма молочных желез (рис. 5).
О возможности влияния тяжелых инфекционных (особенно вирусных) и системных заболеваний, нару шений обменных процессов, интоксикаций, травм ЦНС в период активного становления репродуктив ной системы на половое развитие сообщали многие авторы [1, 2, 3]. Анализ анамнестических данных на ших пациенток в разумной степени подтверждает это утверждение. В основной группе шесть пациенток в возрасте 10–16 лет перенесли туберкулёз лимфати ческих узлов (рис. 6), гепатит «В», гепатит «А», пнев монию, корь, ревмокардит. Невозможно с полной уве ренностью утверждать, что именно эти болезни яви лись причиной гипомастии, однако, подобных приме ров в контрольной группе мы не нашли.
Подобным образом патогенные и наследственные факторы могут воздействовать и на фетальные ткани плода, вызывая множественные врожденные и наслед ственные дефекты, в том числе и молочных желез. В ос нове этих синдромов лежат различного рода диспла зии, чаще эктодермальная и мезенхимальная. Их тяже лые формы крайне редки, а субклинические случаи имеют стёртую симптоматику и сложны в диагностике. В литературе описываются случаи врожденных гипо мастий в сочетании с другими врожденными дефекта ми костной и соединительной ткани, кожи и её произ водных [10, 11, 13, 14]. В наше исследование мы вклю чили пациенток без грубой врожденной патологии, учи тывая при этом любые признаки врожденности, сочета ющиеся с гипомастией и описанные в литературе. Ре шающее значение имели костные деформации грудно го скелета (особенно экскавация грудины, в меньшей степени её килевидная деформация, еще меньше ки фоз, сколиоз, «синдром прямой спины»), пролапс мит рального клапана, дефекты кожи (многочисленные пиг ментные пятна типа веснушек), наличие семейного анамнеза гипомастии. Так же к нарушениям врожденно го генеза мы относим односторонние гипомастии при условии отсутствия воздействия на маммогенез внеш них повреждающих факторов. Самая распространенная деформация в обеих группах – сколиоз (42 и 32 %). Хо тя в основной группе этот процент выше, мы не стали придавать этому большого значения. Гораздо более важным оказалось наличие у пяти пациенток основной группы деформаций грудины по типу экскавации и у од ной – килевидной, а так же наличие подтвержденного пролапса митрального клапана у трёх пациенток и мно жественной кожной пигментации по типу веснушек у двух пациенток (рис. 7–9). У одной пациентки основной группы гипомастия носила явный семейный характер. В контрольной группе нами выявлена только килевидная деформация грудины у трех пациенток.
Анализируя данные результаты, можно сделать одно значный вывод, частота врожденных дефектов в направ лении «умеренная гипомастия – выраженная гипомас тия – микромастия» увеличивается. Соответственно до ля гипомастий, имеющих врожденный генез, увеличи вается в том же направлении. Это утверждение верно в том случае, если дефицит тканей молочных желез свя зан с сопутствующим врожденным дефектом патогене тически. Интересен тот факт, что в основной группе вы явлен более неблагоприятный семейный анамнез по раку молочной железы (четыре пациентки против одной в контрольной группе). Это так же может свидетельство

Рис. 7. Пациентка Л., 32 года, врожденная гипомастия, экскавация нижней трети грудины, нормальная функция молочных желез Fig. 7. Patient L., aged 32 years, with congenital hypomastia, excavation of the lower third of the sternum and normal function of mammary glands

Рис. 8. Пациентка З., 22 года, врожденная гипомастия, пролапс митрального клапана, правосторонний неротационный сколиоз Fig. 8. Patient Z., aged 22 years, with congenital hypomastia, mitral valve prolapse, and rightand side nonrotational scoliosis Рис. 9. Пациентка С., 31 год, врожденная гипомастия, пролапс митрального клапана, множественные пигментные пятна, в семейном анамнезе рак молочной железы Fig. 9. Patient S., aged 31 years, with congenital hypomastia, mitral valve prolapse, multiple pigmentary spots, and breast

cancer in the family history
вать о большей роли врожденных и генетических факто ров в патогенезе выраженных гипомастий.
У всех пациенток с врожденной гипомастией в обе их группах имеющих детей сохранена способность к лактации. Повидимому, это связано с тем, что собст венно железистая ткань сохраняет свою функцию, а дефицит объёма больше связан с дефицитом соеди нительнотканного компонента железы.
У основной массы пациентов обеих групп отсутство вали какиелибо иные отклонения, кроме гипомастии. Большая часть из них обратилась с жалобами на уменьшение объёма и ухудшение формы желез после родов и лактации. Это связано с инволютивной гипот рофией молочных желез, в основе которой лежит пре обладание процессов апоптоза, обратной дифферен цировки железистой ткани, редукции перигландуляр ной стромы и замещения железистой ткани жировой. Уже начиная с 25 летнего возраста, у рожавших жен щин в молочных железах преобладают процессы ин волюции, а к 40 годам они отмечаются как у рожавших, так и у нерожавших женщин. В этой связи инволютив ную гипотрофию принято делить на постлактационную и возрастную. Однако существует группа пациенток с дефицитом объёма молочных желез, которые, не имея явных признаков врожденной патологии, нару шений гормонального статуса, задержки полового развития или инволютивных изменений, по сути, оста ются за рамками нашей систематизации. Нарушени ям такого типа мы дали определение идиопатической гипоплазии (при условии нарушенной функции желе зы) или эстетической гипомастии (в случае если фун кция сохранена) (рис. 10) и выделили в отдельную ка тегорию – дефицит объёма молочных желез неуста новленного генеза.

В итоге, пациенток каждой группы мы разделили на 5 категорий гипомастии (1я категория – ассоцииро ванная с другими врожденными дефектами развития или имеющая наследственный характер (одноили двухсторонняя); 2я – ассоциированная с наруше нием или задержкой полового развития, или наруше нием нейрогуморального гомеостаза; 4я – без явных признаков врождённой патологии, нарушения гормо нального статуса или полового развития, инволютив ных изменений (см. таблицу).
Под понятием гипомастия мы понимаем только де фицит объёма тканей молочной железы. Говоря о ги поплазии, мы имеем в виду комплекс признаков: де фицит объёма, морфологическую незрелость тканей и нарушение функции. В ситуациях, когда невозмож но оценить морфофункциональное состояние молоч ной железы, мы допускаем применение термина ги помастия.
Таким образом, основу контрольной группы соста вили пациентки с постлактационной инволютивной гипотрофией. Большую же часть основной группы за
Таблица. Распределение пациентов основной и контрольной групп по категориям
| Категория | Группа | |||
|---|---|---|---|---|
| основная | контрольная | |||
| 1. Врожденная | 1.1 Гипомастия | 12 (31,6%) | 3 (9,7%) | |
| 1.2 Гипоплазия | – | – | ||
| 2. Первичная | 2.1 Гипомастия | 1 (2,6%) | – | |
| 2.2 Гипоплазия | – | – | ||
| 3. Вторичная | 3.1 Посттравматическая | 3.1.1 гипомастия | – | – |
| 3.1.2 гипоплазия | – | – | ||
| 3.2 Ятрогенная | 3.2.1 гипомастия | 3 (7,9%) | – | |
| 3.2.2 гипоплазия | 1 (2,6) | – | ||
| 4. Неустановленная | 4.1 Эстетическая гипомастия | 8 (21,1%) | 7 (22,6%) | |
| 4.2 Идиопатическая гипоплазия | 2 (5,3%) | – | ||
| 5. Инволютивная гипотрофия | 5.1 Постлактационная | 10 (26,3%) | 21 (67,7%) | |
| 5.2 Возрастная | 1 (2,6%) | – | ||
| Всего: | 38 | 31 | ||
няли пациентки с врожденной гипомастией и в мень шей степени с постлактационной инволютивной ги потрофией.
Выводы
Проводя ретроспективный анализ небольшой группы пациентов, оперированных по поводу дефи цита объёма молочных желез, мы не могли получить более точные результаты, чем те, которые пред ставлены в нашем исследовании. Однако и эти ре зультаты позволяют сделать некоторые выводы, первый и главный из которых состоит в том, что вы раженной гипомастии чаще сопутствует врожден ная патология. Несмотря на единственный выяв ленный случай первичной гипомастии, при более тщательном исследовании гормонального статуса наших пациентов, возможно, их оказалось бы боль ше. Даже на основании анамнестических и физи кальных данных можно определить пациентку в ту или иную группу гипомастии, обосновать и сформу лировать полноценный диагноз. При выраженном дефиците объёма тканей молочных желез и, осо бенно при микромастии, чаще всего имеется при чина этого дефекта. К сожалению, не всегда воз можно достоверно её установить, но можно конста тировать её существование. Этот вопрос требует более фундаментального изучения и, несомненно, большой вклад в понимание механизмов формиро вания, развития молочных желез и, собственно па тогенеза, внесут последние исследования в облас ти человеческого генома, молекулярной биологии и факторов роста. На данный же момент реальной альтернативы хирургическому лечению гипомастии мы не видим. Однако всегда надо учитывать, что ги помастия, а особенно микромастия, могут быть проявлением соматического патологического про цесса, что в корне может повлиять на принятие ре шения об эстетической коррекции данных состоя ний молочных желез.
ЛИТЕРАТУРА
- Коколина В.Ф. Гинекологическая эндокринология детско го и подросткового возраста: Руководство для врачей / 4е изд., перераб., доп. – М.: ИД МЕДПРАКТИКАМ, 2005, 340 с.
- Малыхина Т.В. Отдельные физиологические аспекты вли яния гормонов на процессы в молочных железах // Вестник СамГУ – Естественнонаучная серия. – 2006. – № 6/2 (46). – 178–188 с.
- Сметник В.П. Половые гормоны и молочная железа (обзор литературы) // Гинекология. – Т. 2. – № 5. – 2000.
- Маммопластика при нарушениях объёма и формы молоч ной железы / В.М. Тимербулатов, О.С. Попов, В.В. Плечев, О.В. Попова. – М.: ТриадаХ, 2002. – 176 с.
- Coumoul X., ChuXia Deng. Roles of FGF Receptors in
Mammalian Development and Congenital Diseases // Birth Defects Res. – (Part C). – V. 69. – P. 286–304. – 2003
- Foley J, Dann P, Hong J, Cosgrove J, Dreyer B, Rimm D, et al. Parathyroid hormonerelated protein maintains mammary еpithe lial fate and triggers nipple skin differentiation during embryonic breast development // Development 2001;128: 513–25.
- Herynk Matthew H., Ph.D, and Fuqua Suzanne A. W., Ph. D. Estrogen Receptor Mutations in Human Disease // Endocr. Rev.
– Vol. 25: 869898. – Dec. – 2004.
8. Ishida L.H., Alves H.R.N., Munhoz A.M., Kaimoto C., Ishida L.C., Saito F.L., Gemperlli R., Ferreira M.C. Athelia: case report and review of the literature// British Journal of Plastic Surgery (2005) 58, 833–837
- Lin, K.Y., Nguyen, D.B., and Williams, R.M. Complete breast absence revisited // Plast. Reconstr. Surg. 106: 98, 2000
- Malcolm A. D. Mitral valve prolapse associated with other dis orders. Casual coincidence, common link, or fundamental genetic disturbance? // Br. Heart J. 1985 April; 53(4): 353–362
- Rosenberg C.A., Derman G.H., Grabb W.C., Buda A.J. Hypomastia and mitralvalve prolapse. Evidence of a linked embryologic and mesenchymal dysplasia. // N. Engl. J. Med. 1983; 309:12302.
- Sadove A.M., Van Aalst J.A. Congenital and Acquired Pediatric Breast Anomalies// Plastic and reconstructive surgery,
2005, April 1, p. 10391050.
- Strewler Gordon J., M.D. The Physiology of Parathyroid HormoneRelated Protein // The NEW ENGLAND JOURNAL of MEDICINE Vol. 342:177185
- Wysolmerski John J., Cormier Sarah, Philbrick William M., Dann Pamela, Zhang JianPing, Roume Joelle, Delezoide AnneLise and Silve Caroline Absence of Functional Type 1 Parathyroid Hormone (PTH)/PTHRelated Protein Receptors in Humans Is Associated with Abnormal Breast Development and Tooth Impaction // The Journal of Clinical Endocrinology & Metabolism.
– Vol. 86. – № 4. – Р. 17881794. – 2001.
Гипомастия: принципы систематизации и построения диагноза
Акад. РАМН проф. Н.О. МИЛАНОВ1, О.Л. НИКИТИН, А.Г. ЛИ, Ю.В. БЕЛОВА, Л.Г. КОРНИЕНКО ГУ РНЦХ им. акад. Б.В. Петровского РАМН
Введение
В эстетической хирургии понятие нормы весьма условно и, в то же время, вполне конкретно непосред ственно для пациента. Однако мало кто будет спорить с тем фактом, что состояния, сопровождающиеся вы раженным дефицитом объёма молочных желез, дале ки от нормы. Объединяя эти нарушения общим тер мином – гипомастия, мы имеем в виду лишь внешнюю эстетическую составляющую, опуская индивидуаль ные морфофункциональные особенности и причин ные факторы. Основываясь на метрических парамет рах молочных желез, существующие классификации носят больше прикладной характер, нежели клини ческий. С хирургической точки зрения такой подход вполне объясним и оправдан, однако этого не всегда достаточно для построения полноценного диагноза.
Отдельные состояния, сопровождающиеся гипо мастией в рамках врожденных и эндокринных синд ромов и заболеваний, изучены и описаны в литерату ре достаточно подробно [1, 5, 6, 10, 14], однако, об щей этиопатогенетической систематизации состоя ний, характеризующихся дефицитом объёма тканей молочных желез на данный момент нет. По нашему мнению, этому есть несколько причин:
• отсутствие четких этиопатогенетических крите риев гипомастии;
1Н.О. МИЛАНОВ Россия, 119992, Москва, Абрикосовский пер., 2 Тел: (495) 248 16 15, факс: (495) 248 60 77 Email: milanov@med.ru
Hypomastia: principles of systematization and diagnosis
Professor N.O. MILANOV1, member of Russian Academy of Medical Sciences, O.L NIKITIN, A.G. LEE, Yu.V. BELOVA,
L.G. KORNIENKO
B.V. Petrovsky State Research Centre of Surgery, Russian Academy of Medical Sciences
- сложность и малоизученность тонких механизмов регуляции развития молочных желез;
- многообразие факторов, приводящих к наруше нию этих механизмов;
- высокая вариабельность морфологических ха рактеристик не только у разных женщин, но у од ной и той же в разные периоды жизни и цикла.
В своём исследовании мы попытались оценить группу пациентов с выраженной гипомастией с пози ций этиопатогенеза и, исходя из результатов, сфор мулировать наиболее общие аспекты систематиза ции данных нарушений и построения диагноза.
Материалы и методы
В исследование мы включили две группы пациен тов. В первую, основную группу, мы включили 38 па циенток с выраженной гипомастией, которым была выполнена первичная увеличивающая маммопласти ка. Во вторую группу, которую мы рассматривали как контрольную, мы включили 31 пациентку, которым также была выполнена первичная увеличивающая маммопластика. Критериями отбора пациенток в ос новную группу стали: выраженный одно или двухсто ронний дефицит объёма тканей молочных желез, со храненный сосковоареолярный комплекс и отсутст вие четко визуализируемой субмаммарной дуги или
1N.O. Milanov Abrikosovsky per., 2, 119992 Moscow, Russia Tel.: (495) 248 16 15; fax: (495) 248 60 77 email: milanov@med.ru
складки. В контрольную группу мы включили пациен ток с умеренной гипомастией без птоза.
Анализ пациентов проводили ретроспективно. Оце нивали наличие и характер врожденных дефектов и пороков развития, гормональных нарушений, функ циональное состояние молочных желез, общее физи ческое развитие, сопутствующие и перенесенные за болевания. Оценку проводили на основании анам нестических данных и данных физикального обследо вания пациенток. При необходимости и по показани ям дополнительно производили инструментальные и лабораторные исследования. В анализе результатов исследования решающее значение придавалось установленной и описанной в литературе связи неко торых выявленных дефектов развития и сопутствую щих заболеваний с гипомастией [5, 8–11].
В основу систематизации так же положены три ос новных понятия: гипомастия, гипоплазия и гипотрофия.
Результаты и обсуждение
Возраст пациенток, оперированных по поводу гипо мастии и вошедших в исследование, колебался от 18 до 42 лет. Средний возраст пациенток основной груп пы составил 27 лет, контрольной – 30 лет.
В основной группе семь пациенток имели выра женную одностороннюю гипомастию с асимметрией молочных желез. Причина гипомастии у четверых из них – хирургическое вмешательство на грудной клет ке в области одной из молочных желез – три наблю дения (рис. 1), и лучевая терапия в детском возрас те – одно наблюдение (рис. 2). Односторонняя гипо
Рис. 1. Пациентка Н., 22 года, вторичная ятрогенная гипомастия справа, вторичная приобретенная асимметрия молочных желез, в возрасте 8 мес оперирована по поводу гемангиомы правой молочной железы Fig. 1. Patient N., aged 22 years, with righthand side secondary iatrogenic hypomastia and secondary acquired breast asymmetry. The patient was operated at the age of 8 years for right breast hemangioma
Рис. 2. Пациентка П., 20 лет, вторичная ятрогенная гипоплазия молочной железы справа, вторичная приобретенная асимметрия молочных желез, лучевая терапия в детском возрасте Fig. 2. Patient P., aged 20 years, secondary iatrogenic hypoplasia of the right breast and secondary acquired breast asymmetry. The patient underwent radiotherapy when a child Рис. 3. Пациентка Б., врожденная гипомастия справа, врожденная асимметрия молочных желез Fig. 3. Patient B. with righthand side congenital hypomastia and congenital breast asymmetry
Рис. 4. Пациентка А., 18 лет, первичная гипомастия, диффузное увеличение щитовидной железы II степени, эутиреоз, гиперандрогения, генитальный инфантилизм Fig. 4. Patient A., aged 18 years, with primary hypomastia, grade II diffuse enlargement of the thyroid gland, euthyroidism,
hyperandrogenism, and genital infantilism
мастия у остальных трех пациенток была врожденно го генеза (рис. 3).
Оценивая функциональное состояние молочных желез пациенток обеих групп, надо отметить, что из 17 (45 %) рожавших пациенток основной группы не смотря на выраженный дефицит объёма тканей мо лочных желез – только у двух не было лактации. В кон трольной группе никто из 23 (74%) пациенток, имею щих детей, на отсутствие лактации не жаловался.
Обращает на себя внимание тот факт, что количест во родов доношенным плодом в группе выраженных гипомастий – заметно ниже. Это могло бы свидетель ствовать о возможных гормональных нарушениях и незрелости репродуктивной системы, однако, мы не склонны придавать этому решающее значение, учи тывая, что данные могут несколько искажаться факто рами социального и психологического плана, играю щими особую роль в жизни пациенток с выраженным дефицитом объёма молочных желез [4].
В одном наблюдении у пациентки 18 лет, включен ной в основную группу, выявлена эндокринная пато логия с нарушением гормонального статуса в виде гиперандрогении и изменения уровня оборотных гор монов щитовидной железы, приведшая к дисгормо нальному половому развитию, половому инфантилиз му и микромастии (рис. 4). В данном наблюдении вы явлен эутиреоз с диффузным увеличением щитовид ной железы II степени, по поводу чего пациентка на блюдалась у эндокринолога. Надо отметить, что именно в период полового созревания любые нару шения нейрогуморального гомеостаза крайне пагуб но влияют на половое развитие и развитие молочных желез в частности [1, 2]. Хорошей иллюстрацией тому служит пример двух пациенток контрольной группы
Рис. 5. Пациентка В., 28 лет, эстетическая гипомастия, сопутствующая патология – узловой эутиреоидный зоб, выявлен к 28 годам Fig. 5. Patient C., aged 28 years, with aesthetically unacceptable hypomastia and concurrent euthyroid nodular goiter diagnosed at the age of 28 years
Рис. 6. Пациентка Б., 26 лет, эстетическая гипомастия, туберкулёз лимфоузлов в анамнезе Fig. 6. Patient B., aged 26 years, with aesthetically unacceptable hypomastia and the history of lymph node tuberculosis
28 и 32 лет с патологией щитовидной железы, забо левших уже будучи взрослыми и не имеющих значи тельного нарушение объёма молочных желез (рис. 5).
О возможности влияния тяжелых инфекционных (особенно вирусных) и системных заболеваний, нару шений обменных процессов, интоксикаций, травм ЦНС в период активного становления репродуктив ной системы на половое развитие сообщали многие авторы [1, 2, 3]. Анализ анамнестических данных на ших пациенток в разумной степени подтверждает это утверждение. В основной группе шесть пациенток в возрасте 10–16 лет перенесли туберкулёз лимфати ческих узлов (рис. 6), гепатит «В», гепатит «А», пнев монию, корь, ревмокардит. Невозможно с полной уве ренностью утверждать, что именно эти болезни яви лись причиной гипомастии, однако, подобных приме ров в контрольной группе мы не нашли.
Подобным образом патогенные и наследственные факторы могут воздействовать и на фетальные ткани плода, вызывая множественные врожденные и наслед ственные дефекты, в том числе и молочных желез. В ос нове этих синдромов лежат различного рода диспла зии, чаще эктодермальная и мезенхимальная. Их тяже лые формы крайне редки, а субклинические случаи имеют стёртую симптоматику и сложны в диагностике. В литературе описываются случаи врожденных гипо мастий в сочетании с другими врожденными дефекта ми костной и соединительной ткани, кожи и её произ водных [10, 11, 13, 14]. В наше исследование мы вклю чили пациенток без грубой врожденной патологии, учи тывая при этом любые признаки врожденности, сочета ющиеся с гипомастией и описанные в литературе. Ре шающее значение имели костные деформации грудно го скелета (особенно экскавация грудины, в меньшей степени её килевидная деформация, еще меньше ки фоз, сколиоз, «синдром прямой спины»), пролапс мит рального клапана, дефекты кожи (многочисленные пиг ментные пятна типа веснушек), наличие семейного анамнеза гипомастии. Так же к нарушениям врожденно го генеза мы относим односторонние гипомастии при условии отсутствия воздействия на маммогенез внеш них повреждающих факторов. Самая распространенная деформация в обеих группах – сколиоз (42 и 32 %). Хо тя в основной группе этот процент выше, мы не стали придавать этому большого значения. Гораздо более важным оказалось наличие у пяти пациенток основной группы деформаций грудины по типу экскавации и у од ной – килевидной, а так же наличие подтвержденного пролапса митрального клапана у трёх пациенток и мно жественной кожной пигментации по типу веснушек у двух пациенток (рис. 7–9). У одной пациентки основной группы гипомастия носила явный семейный характер. В контрольной группе нами выявлена только килевидная деформация грудины у трех пациенток.
Анализируя данные результаты, можно сделать одно значный вывод, частота врожденных дефектов в направ лении «умеренная гипомастия – выраженная гипомас тия – микромастия» увеличивается. Соответственно до ля гипомастий, имеющих врожденный генез, увеличи вается в том же направлении. Это утверждение верно в том случае, если дефицит тканей молочных желез свя зан с сопутствующим врожденным дефектом патогене тически. Интересен тот факт, что в основной группе вы явлен более неблагоприятный семейный анамнез по раку молочной железы (четыре пациентки против одной в контрольной группе). Это так же может свидетельство
Рис. 7. Пациентка Л., 32 года, врожденная гипомастия, экскавация нижней трети грудины, нормальная функция молочных желез Fig. 7. Patient L., aged 32 years, with congenital hypomastia, excavation of the lower third of the sternum and normal function of mammary glands
Рис. 8. Пациентка З., 22 года, врожденная гипомастия, пролапс митрального клапана, правосторонний неротационный сколиоз Fig. 8. Patient Z., aged 22 years, with congenital hypomastia, mitral valve prolapse, and righthand side nonrotational scoliosis Рис. 9. Пациентка С., 31 год, врожденная гипомастия, пролапс митрального клапана, множественные пигментные пятна, в семейном анамнезе рак молочной железы Fig. 9. Patient S., aged 31 years, with congenital hypomastia, mitral valve prolapse, multiple pigmentary spots, and breast
cancer in the family history
вать о большей роли врожденных и генетических факто ров в патогенезе выраженных гипомастий.
У всех пациенток с врожденной гипомастией в обе их группах имеющих детей сохранена способность к лактации. Повидимому, это связано с тем, что собст венно железистая ткань сохраняет свою функцию, а дефицит объёма больше связан с дефицитом соеди нительнотканного компонента железы.
У основной массы пациентов обеих групп отсутство вали какиелибо иные отклонения, кроме гипомастии. Большая часть из них обратилась с жалобами на уменьшение объёма и ухудшение формы желез после родов и лактации. Это связано с инволютивной гипот рофией молочных желез, в основе которой лежит пре обладание процессов апоптоза, обратной дифферен цировки железистой ткани, редукции перигландуляр ной стромы и замещения железистой ткани жировой. Уже начиная с 25 летнего возраста, у рожавших жен щин в молочных железах преобладают процессы ин волюции, а к 40 годам они отмечаются как у рожавших, так и у нерожавших женщин. В этой связи инволютив ную гипотрофию принято делить на постлактационную и возрастную. Однако существует группа пациенток с дефицитом объёма молочных желез, которые, не имея явных признаков врожденной патологии, нару шений гормонального статуса, задержки полового развития или инволютивных изменений, по сути, оста ются за рамками нашей систематизации. Нарушени ям такого типа мы дали определение идиопатической гипоплазии (при условии нарушенной функции желе зы) или эстетической гипомастии (в случае если фун кция сохранена) (рис. 10) и выделили в отдельную ка тегорию – дефицит объёма молочных желез неуста новленного генеза.
В итоге, пациенток каждой группы мы разделили на 5 категорий гипомастии (1я категория – ассоцииро ванная с другими врожденными дефектами развития или имеющая наследственный характер (одно или двухсторонняя); 2я – ассоциированная с наруше нием или задержкой полового развития, или наруше нием нейрогуморального гомеостаза; 4я – без явных признаков врождённой патологии, нарушения гормо нального статуса или полового развития, инволютив ных изменений (см. таблицу).
Под понятием гипомастия мы понимаем только де фицит объёма тканей молочной железы. Говоря о ги поплазии, мы имеем в виду комплекс признаков: де фицит объёма, морфологическую незрелость тканей и нарушение функции. В ситуациях, когда невозмож но оценить морфофункциональное состояние молоч ной железы, мы допускаем применение термина ги помастия.
Таким образом, основу контрольной группы соста вили пациентки с постлактационной инволютивной гипотрофией. Большую же часть основной группы за
Таблица. Распределение пациентов основной и контрольной групп по категориям
| Категория | Группа | |||
|---|---|---|---|---|
| основная | контрольная | |||
| 1. Врожденная | 1.1 Гипомастия | 12 (31,6%) | 3 (9,7%) | |
| 1.2 Гипоплазия | – | – | ||
| 2. Первичная | 2.1 Гипомастия | 1 (2,6%) | – | |
| 2.2 Гипоплазия | – | – | ||
| 3. Вторичная | 3.1 Посттравматическая | 3.1.1 гипомастия | – | – |
| 3.1.2 гипоплазия | – | – | ||
| 3.2 Ятрогенная | 3.2.1 гипомастия | 3 (7,9%) | – | |
| 3.2.2 гипоплазия | 1 (2,6) | – | ||
| 4. Неустановленная | 4.1 Эстетическая гипомастия | 8 (21,1%) | 7 (22,6%) | |
| 4.2 Идиопатическая гипоплазия | 2 (5,3%) | – | ||
| 5. Инволютивная гипотрофия | 5.1 Постлактационная | 10 (26,3%) | 21 (67,7%) | |
| 5.2 Возрастная | 1 (2,6%) | – | ||
| Всего: | 38 | 31 | ||
няли пациентки с врожденной гипомастией и в мень шей степени с постлактационной инволютивной ги потрофией.
Выводы
Проводя ретроспективный анализ небольшой группы пациентов, оперированных по поводу дефи цита объёма молочных желез, мы не могли получить более точные результаты, чем те, которые пред ставлены в нашем исследовании. Однако и эти ре зультаты позволяют сделать некоторые выводы, первый и главный из которых состоит в том, что вы раженной гипомастии чаще сопутствует врожден ная патология. Несмотря на единственный выяв ленный случай первичной гипомастии, при более тщательном исследовании гормонального статуса наших пациентов, возможно, их оказалось бы боль ше. Даже на основании анамнестических и физи кальных данных можно определить пациентку в ту или иную группу гипомастии, обосновать и сформу лировать полноценный диагноз. При выраженном дефиците объёма тканей молочных желез и, осо бенно при микромастии, чаще всего имеется при чина этого дефекта. К сожалению, не всегда воз можно достоверно её установить, но можно конста тировать её существование. Этот вопрос требует более фундаментального изучения и, несомненно, большой вклад в понимание механизмов формиро вания, развития молочных желез и, собственно па тогенеза, внесут последние исследования в облас ти человеческого генома, молекулярной биологии и факторов роста. На данный же момент реальной альтернативы хирургическому лечению гипомастии мы не видим. Однако всегда надо учитывать, что ги помастия, а особенно микромастия, могут быть проявлением соматического патологического про цесса, что в корне может повлиять на принятие ре шения об эстетической коррекции данных состоя ний молочных желез.
ЛИТЕРАТУРА
- Коколина В.Ф. Гинекологическая эндокринология детско го и подросткового возраста: Руководство для врачей / 4е изд., перераб., доп. – М.: ИД МЕДПРАКТИКАМ, 2005, 340 с.
- Малыхина Т.В. Отдельные физиологические аспекты вли яния гормонов на процессы в молочных железах // Вестник СамГУ – Естественнонаучная серия. – 2006. – № 6/2 (46). – 178–188 с.
- Сметник В.П. Половые гормоны и молочная железа (обзор литературы) // Гинекология. – Т. 2. – № 5. – 2000.
- Маммопластика при нарушениях объёма и формы молоч ной железы / В.М. Тимербулатов, О.С. Попов, В.В. Плечев, О.В. Попова. – М.: ТриадаХ, 2002. – 176 с.
- Coumoul X., ChuXia Deng. Roles of FGF Receptors in
Mammalian Development and Congenital Diseases // Birth Defects Res. – (Part C). – V. 69. – P. 286–304. – 2003
- Foley J, Dann P, Hong J, Cosgrove J, Dreyer B, Rimm D, et al. Parathyroid hormonerelated protein maintains mammary еpithe lial fate and triggers nipple skin differentiation during embryonic breast development // Development 2001;128: 513–25.
- Herynk Matthew H., Ph.D, and Fuqua Suzanne A. W., Ph. D. Estrogen Receptor Mutations in Human Disease // Endocr. Rev.
– Vol. 25: 869898. – Dec. – 2004.
8. Ishida L.H., Alves H.R.N., Munhoz A.M., Kaimoto C., Ishida L.C., Saito F.L., Gemperlli R., Ferreira M.C. Athelia: case report and review of the literature// British Journal of Plastic Surgery (2005) 58, 833–837
- Lin, K.Y., Nguyen, D.B., and Williams, R.M. Complete breast absence revisited // Plast. Reconstr. Surg. 106: 98, 2000
- Malcolm A. D. Mitral valve prolapse associated with other dis orders. Casual coincidence, common link, or fundamental genetic disturbance? // Br. Heart J. 1985 April; 53(4): 353–362
- Rosenberg C.A., Derman G.H., Grabb W.C., Buda A.J. Hypomastia and mitralvalve prolapse. Evidence of a linked embryologic and mesenchymal dysplasia. // N. Engl. J. Med. 1983; 309:12302.
- Sadove A.M., Van Aalst J.A. Congenital and Acquired Pediatric Breast Anomalies// Plastic and reconstructive surgery,
2005, April 1, p. 10391050.
- Strewler Gordon J., M.D. The Physiology of Parathyroid HormoneRelated Protein // The NEW ENGLAND JOURNAL of MEDICINE Vol. 342:177185
- Wysolmerski John J., Cormier Sarah, Philbrick William M., Dann Pamela, Zhang Jianing, Roume Joelle, Delezoide AnneLise and Silve Caroline Absence of Functional Type 1 Parathyroid Hormone (PTH)/PTHRelated Protein Receptors in Humans Is Associated with Abnormal Breast Development and Tooth Impaction // The Journal of Clinical Endocrinology & Metabolism.
– Vol. 86. – № 4. – Р. 17881794. – 2001.
Отзывы
Все отзывы »